Quote:
Originariamente inviata da zicchinet
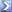
L' Acido Ascorbico (vitaminaC) reagisce con I3- formando l'acido deidroascorbico. Nella reazione è utilizzato come indicatore l'amido. Il punto finale è contrassegnato dalla scomparsa di un complesso amido-iodio blu scuro quando la prima goccia di I3- non reagito rimane in soluzione.
A) Se per reagire con 0,1970g di A.ascorbico puro sono necessari 29,41 mL di una soluzione I3-, qual'è la della soluzione I3-?
B) Una compressa di vitamina C contenente acido ascorbico più un legante inerte è stata macinata e ridotta in polvere, e se ne sono titolati 0,4242g con 31,63 mL di I3-, trovare la percentuale in peso di acido ascorbico nella compressa.
|
C6H8O6 + I3- = C6H6O6 + 3 I - + 2H+
(ac.L+ascorbico + triioduro = ac.deidroascorbico)
il rapporto di combinazione è 1:1
quindi
mmoli(C6H8O6) = mmol(I3-)
=
197mg / PM(=176g/mol) = 1.12mmol = 29.41mL * M
=> a) M = 1.12mmol/29.41mL = 0.038M
b) mmoli(C6H8O6) = mmol(I3-) = 31.63mL * 0.038M = 1.20mmol
1.20mmol * PM = 211.9mg
211.9mg / 424.2mg * 100 = 49.95%
__________________
Lezioni e svolgimento di esercizi di CHIMICA on line!
http://chimicaonline.xoom.it
Sono anche su facebook, ID: Lachimica On Line
